Tăng nhu cầu ghép gan ở bệnh nhân ung thư gan
1- Tái phát sau khi chữa khỏi viêm gan C có thể do nhiễm virus tiềm tàng
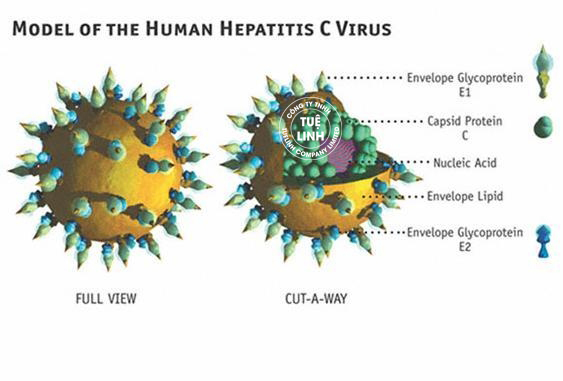
Hình ảnh virus viêm gan C
Những người tái phát bệnh sau khoảng thời gian dài chữa khỏi viêm gan C (HCV) có thể không phải do nhiễm chủng virus khác mà là sự xuất hiện trở lại của virus cũ. Trong nghiên cứu được đăng trên tạp chí Bệnh nhiễm trùng, các nhà nghiên cứu đã phân tích trình tự RNA trong cả huyết thanh và tế bào gan của 103 bệnh nhân tham gia nghiên cứu đã từng đạt đáp ứng virus (đáp ứng được coi là chữa khỏi) sau khi chữa bằng phác đồ chứa interferon từ 1985 đến 2005.
3 bệnh nhân trong nhóm nghiên cứu tái phát muộn, có xét nghiệm HCV (+) sau khi chữa khỏi lần lượt là 8, 75 và 78 tháng. Có 4 bệnh nhân thuộc nhóm chứng tái phát sớm.
Các nhà nghiên cứu phân tích trình tự RNA trong huyết thanh của các bệnh nhân cả trước khi điều trị và sau khi tái phát. Họ thấy rằng có đến 99,4% trình tự trùng nhau giữa 2 mẫu trong số các bệnh nhân tái phát sớm và 99,8% trong số các bệnh nhân tái phát muộn. Chủng virus cũng giống nhau giữa 2 mẫu trong tất cả các trường hợp. Điều này cho thấy không hề có chủng virus mới xuất hiện ở người bệnh bị tái phát muộn.
Các nhà khoa học cho rằng HCV có thể trú ngụ trong gan sau khi đạt được đáp ứng virus. Các nghiên cứu cần được tiến hành thêm để xác định tải lượng virus là bao nhiêu thì chúng có thể vẫn tồn tại lâu dài sau khi bệnh được chữa khỏi.
2- Nhu cầu ghép gan tăng ở bệnh nhân ung thư gan do virus viêm gan C
Nhu cầu ghép gan tang cao
Danh sách ghép gan đang ngày càng dài đối với bệnh nhân viêm gan C. Theo Jenifer Flemming thuộc Đại học Queen ở Kingston, Ontario, điều này là do số ca ung thư gan- dạng ung thư gan phổ biến nhất đang tăng trong nhóm bệnh nhân viêm gan C. Kết quả này được báo cáo tại Hội nghị thường niên của Hiệp hội nghiên cứu bệnh gan Hoa Kỳ (AASLD) lần thứ 64 tại Washington DC.
Để nhận thấy xu hướng ghép gan và đưa ra những dự đoán, Flemming và cộng sự đã phân tích các thông tin từ bản đăng ký khoa học của người nhận gan trong khoảng thời gian từ tháng 1/2003 đến tháng 12/2010.
Tổng cộng có 20.325 người viêm gan C đang trong danh sách chờ ghép gan trong giai đoạn này, trong đó có 12.724 người bị bệnh gan giai đoạn cuối và 7.061 người bị ung thư tế bào gan.
Trong số các bệnh nhân viêm gan C, số bệnh nhân ung thư tế bào gan tăng mạnh hơn so với số bệnh nhân bị bệnh gan giai đoạn cuối, điều này có nghĩa là các trường hợp ung thư gan do viêm gan C đang tạo sức ép lên nhu cầu gan để ghép.
Các nhà nghiên cứu ước tính rằng số lượng bệnh nhân viêm gan C phải ghép gan sẽ tăng từ 2.072 ca năm 2013 đến 3.053 ca vào năm 2020, thời điểm số lượng người Mỹ bị ung thư gan, bệnh gan giai đoạn cuối đạt đỉnh. Số lượng người bệnh viêm gan C và bệnh gan giai đoạn cuối sẽ tăng từ 1.451 đến 1.674, và do đó số lượng ca cần ghép gan sẽ tăng từ 623 đến 1.379 ca.
3- FDA cấp phép cho thuốc điều trị viêm gan C mới Sovaldi (sofosbuvir)
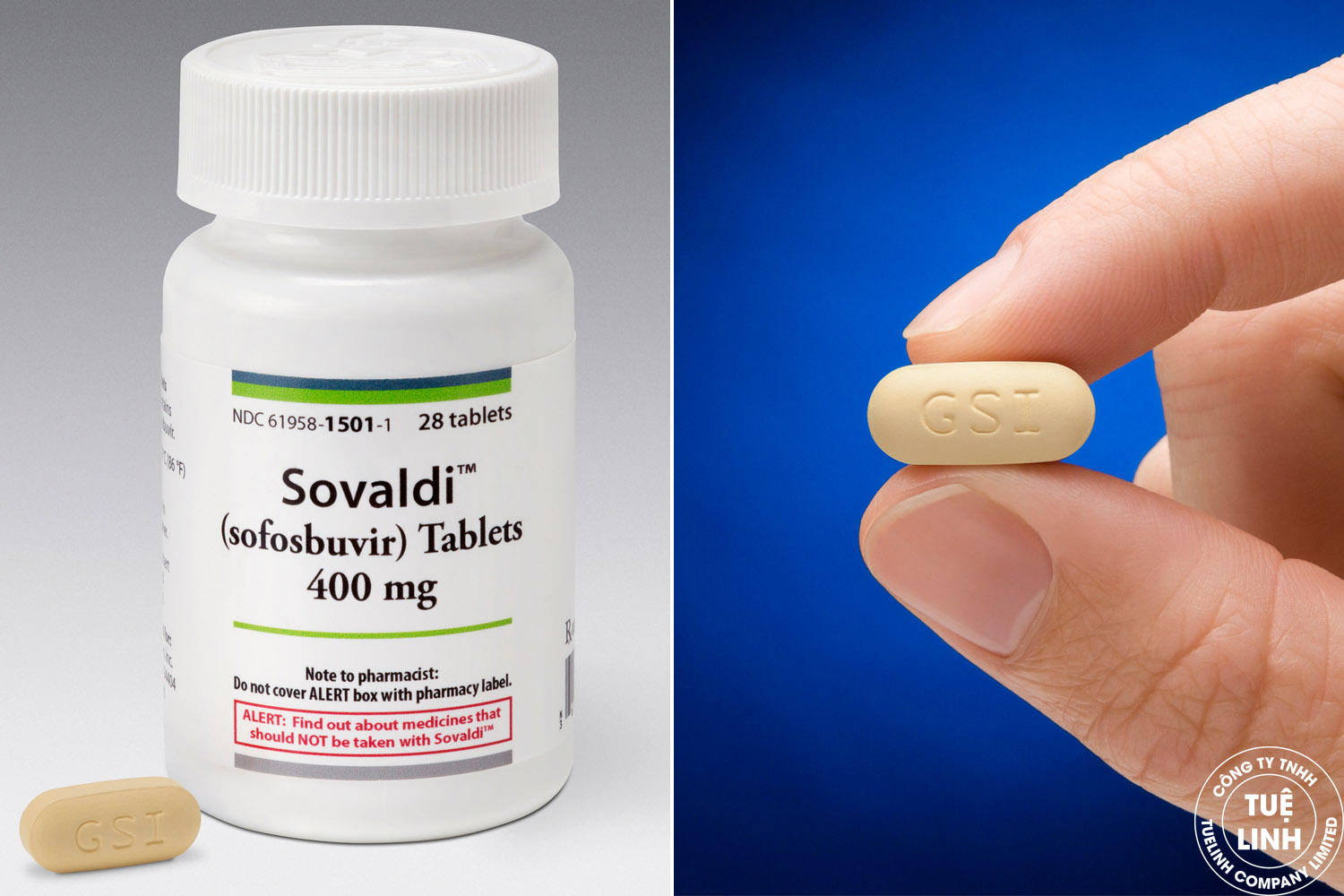
Thuốc điều trị viêm gan C
Cục quản lý thuốc và thực phẩm Hoa Kỳ vừa cho phép thuốc Sovaldi (sofosbuvir) của Gilead Science lưu hành. Đây là thuốc ức chế polymerase có cấu trúc tương tự nucleotide dùng đường uống, ngày một lần để điều trị nhiễm virus viêm gan C (HCV), bao gồm cả bệnh nhân nhiễm HIV và người ung thư gan đang chờ ghép. Đối với bệnh nhân nhiễm HCV tuýp 2 hoặc 3, Sovaldi là thuốc điều trị đầu tiên không cần dùng cùng interferon. Tuy nhiên, bệnh nhân tuýp 1 và 4, trong hầu hết trường hợp, vẫn cần tiêm interferon.
Sovaldi phải dùng cùng với ribavirin cho bất kì tuýp virus nào. Thời gian điều trị khuyến cáo là 12 tuần đối với tuýp 1, 2, 4 và 24 tuần đối với tuýp 3.
Gilead tuyên bố rằng những bệnh nhân tuýp 1 không thể dùng interferon “có thể được xem xét” để dùng Sovaldi và ribavirin trong vòng 24 tuần. Bên cạnh đó, ở người đang chờ ghép gan, phác đồ tương tự nên được dùng trong 48 tuần trước khi ghép để ngăn nhiễm virus sau khi ghép.
“Sự cấp phép hôm nay đánh dấu một bước chuyển lớn trong phác đồ điều trị viêm gan C mạn tính” Edward Cox, tiến sĩ Y học, giám đốc phòng Sản phẩm kháng sinh trong Trung tâm nghiên cứu và đánh giá thuốc của FDA cho biết.
Chi phí dùng Sovaldi trong vòng 4 tuần là 28.000 $. Trong cùng khoảng thời gian này, Olysio- thuốc được FDA cấp phép vào ngày 22/11/2013 là 22.120 $.
Sovaldi là kết quả đầu tiên trong việc nghiên cứu phác đồ điều trị viêm gan C dùng đường uống, không có interferon và thậm chí là cả ribavirin. Tuy nhiên, việc lưu hành Sovaldi, Olysio chỉ là bước khởi đầu. Phác đồ kiểu như thế sẽ không xuất hiện đến cuối năm 2014. Gilead đang hy vọng thuốc phối hợp giữa Sovaldi và ledipasvir (chất ức chế NS5A của công ty này có khả năng chữa khỏi gần như 100% trường hợp trong các thử nghiệm lâm sàng gần đây) sẽ được cấp phép.
Hiện tại, bác sĩ có thể lựa chọn kế đơn Sovaldi kết hợp với Olysio. Nghiên cứu pha 2 lâm sàng phối hợp 2 thuốc này, có dùng hoặc không dùng ribavirin, có thể chữa khỏi trên 90% trường hợp.
FDA cấp phép cho Sovaldi dựa trên dữ liệu từ 4 thử nghiệm lâm sàng pha 3 là NEUTRINO, FISSION, POSITRON và FUSION. Khoảng từ 50 đến 90% người dùng thuốc đạt đáp ứng virus 12 tuần sau khi kết thúc điều trị (SVR12, được coi là chữa khỏi).
Sovaldi có khả năng dung nạp tốt, với một số tác dụng phụ nhẹ. Các tác dụng phổ biến nhất, xảy ra trên 20% ở người bệnh dùng Sovaldi cùng với ribavirin và interferon là mệt mỏi, đau đầu, buồn nôn, mất ngủ và thiếu máu.
Theo tuelinh.vn (tổng hợp)



